- 概述
- 理由
- 解答问题
- 应用指南
- 发表文章
支持脂质膜可以在体外实验中用于模拟主要由磷脂组成的生物屏障,如细胞膜。也可以将其他分子,如受体或膜蛋白结合到脂质层结构中,以模拟生物膜的特定功能。由于这些特性,支撑脂质层结构在生物化学和制药研究领域有着广泛的应用。
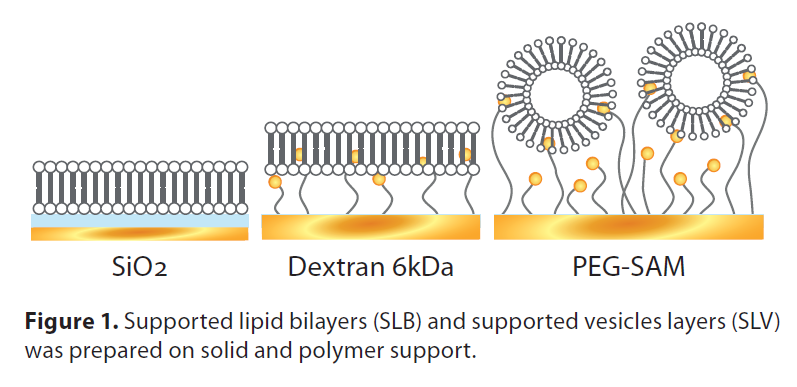
传统的支持脂质双分子层(SLB)或囊泡层(SLV)是在固体载体上制备的,如SiO2或金(Au),但层在通过空气-水界面过渡时往往不稳定。聚合物载体可以提高所形成的脂质层的稳定性。
SPR现象是基于自由电子在金属表面共振,这些电子被光激发。吸收最大值是入射光角度的函数,SPR现象高度依赖于金属表面附近的介电常数。表面附近的任何变化,如脂层的沉积,都能最大程度地改变吸收角度。MP-SPR的独特功能是同时测量两种不同的波长,可以同时计算沉积层的厚度(d)和折射率(RI),而无需事先了解其中任何一种。
材料与方法
合成了两种用于脂质结合的聚合物表面:6 kDa葡聚糖和聚乙二醇自组装单层(PEG-SAM)。我们以SiO2表面作为SLB形成的参比表面(图1)。脂质体的主要成分为EggPC(卵磷脂酰胆碱),因为大多数原核细胞膜都是卵磷脂酰胆碱。添加POPS(棕榈酰油酰磷脂酰丝氨酸)形成天然负电荷和胆固醇,模拟细胞膜的自然刚性。研究了三种不同的脂质组成:100%蛋pc、75:25%蛋pc:POPS和70:25:5%蛋pc:POPS:胆固醇。此外,还研究了HepG2细胞的细胞膜提取物。
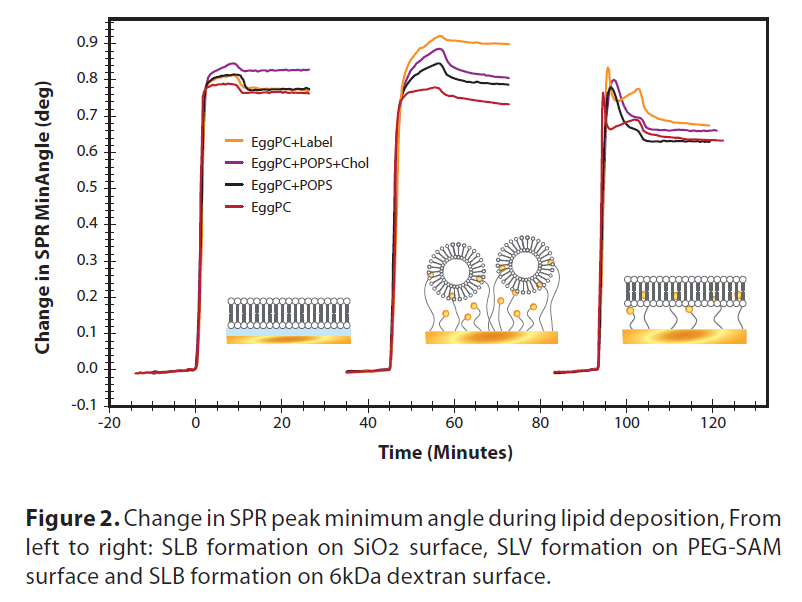
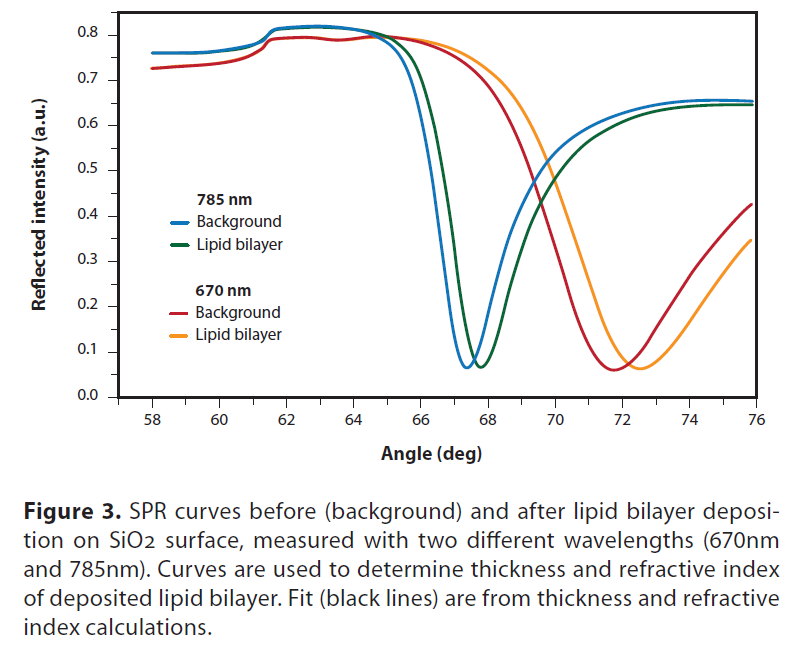
用SPR Navi 200-L测量脂质体与不同表面的相互作用(图2)。还研究了空气-水过渡过程中负载脂双分子层的稳定性。根据脂质体沉积前后的SPR曲线计算形成的脂质层厚度和折射率(RI)(图3)。
结果与讨论
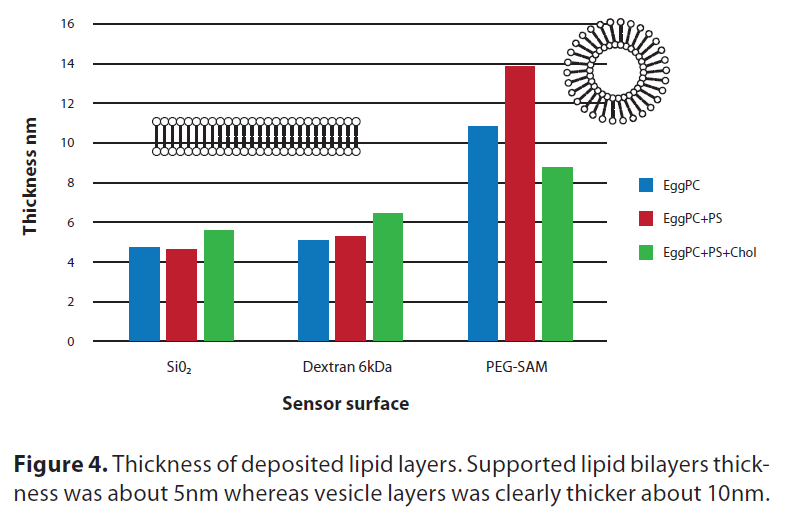
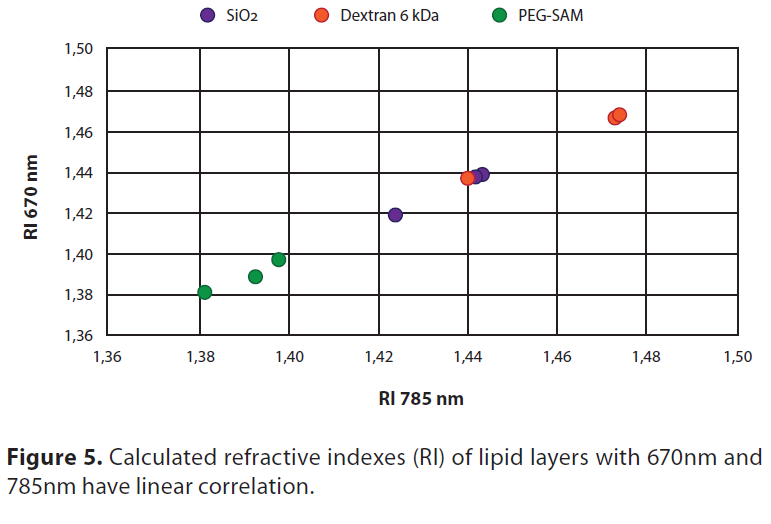
即使6kDa葡聚糖和PEG-SAM都是相对较薄(几纳米)的亲水凝胶载体,葡聚糖表面明显促进SLB的形成,而PEG-SAM支持SLV的形成。计算的厚度和RI值显示右旋糖酐上的脂质层与PEG-SAM上的脂质层有明显差异(图4)。表面促进行为的差异很可能是由于聚合物亲水性基团的密度和位置不同。右旋糖酐支持所使用的三种脂质组合物的脂质双层形成(图4)。
用MP-SPR仪对右旋糖酐表面的胆固醇SLB进行气-水过渡和气流暴露。注意到SLB具有优异的抗干燥性,这是仿生表面的理想特性。与所研究的其他脂质体相比,hepg2 -提取物具有更大的SPR信号,可能是由于其含有膜蛋白和其他成分。
结论
脂质体或脂双分子层形式的支撑脂层可以沉积在SPR传感器载玻片上。MP-SPR是一种在不知道沉积层厚度和折射率的情况下确定沉积层厚度和折射率的独特方法。支持脂质层可以进一步用于药物发现和开发、生物传感和生物物理学等领域,以确定分子与脂质层的相互作用。
