- 概述
- 理由
- 解答问题
- 应用指南
- 发表文章
纳米载体正被广泛研究作为癌症和基因治疗等药物输送系统。研究了嵌段共聚胶束(LMP)作为黏附性眼部给药载体。采用多参数表面等离子体共振(MP-SPR)测定了粘蛋白表面胶束和壳聚糖的相互作用参数。随着纳米颗粒中苯硼酸(PBA)含量的增加,胶束粘附力略有增加。
在另一项研究中,使用MP-SPR测量了C3b分子与脂质体的结合。C3b是先天免疫系统的一部分,它作为一种调理剂增强吞噬作用(更具体地说,标记细胞进行吞噬)。C3b对聚乙二醇化寡聚胍脂质修饰(OGP + PEG)脂质体的亲和力为KD = 7.2 × 10−8 M,表面质量密度Γ = 120 ~ 200 ng/cm2。不含PEG的脂质体上的结合水平较高。
简介
纳米载体的临床安全性可以通过降低其免疫原性或增加其细胞靶向能力来提高。纳米载体也被广泛优化,以改善药物在严密的生物屏障上的传递,这些生物屏障是难以克服的,如血脑和血血管屏障。
表面等离子体共振(SPR)是一种实时、无标记地测量分子相互作用(如药物和蛋白质相互作用)的常用方法。多参数表面等离子体共振(MP-SPR)将SPR的适用性从分子相互作用测量扩展到纳米颗粒/靶标和纳米颗粒/细胞相互作用的更基本的研究,包括材料表征。
MP-SPR仪器可以在宽角度扫描范围(40-78度)和多个波长下进行独特的测量,因此使其成为纳米颗粒和细胞研究的宝贵系统。MP-SPR实时测量吸附,同样的测量允许计算层厚度。此外,MP-SPR Navi™仪器流体很容易调节纳米颗粒和样品的研究,同时仍然保持无堵塞的操作。
MP-SPR仪器的光学设置可以同时测量多个光学参数。参数的相互关系允许使用PureKinetics™功能对干扰体信号进行简单的在线表征,并允许对体进行实时校正。当使用改变缓冲液时,或者当不存在最佳参考表面时,例如在分子或纳米颗粒与脂质层或材料相互作用期间,这是非常有用的。
材料和方法
研究一
合成了一系列嵌段共聚物胶束(LMP =聚(L -丙交酯)-聚(b-聚(甲基丙烯酸-co-3-丙烯酰胺苯基硼酸)),其中苯基硼酸(LMP-0、LMP-5、LMP-10、LMP-20和LMP-30)的用量增加。通过动态光散射测定,脂质体的大小从36 nm (LMP-0)到64 nm (LMP-30)不等。脂质体和壳聚糖在粘蛋白表面相互作用50分钟(图1.A)。以壳聚糖(1 mg/mL)相互作用为阳性对照,观察其对粘膜粘附的影响。在100 μg/mL牛颌下腺粘蛋白(4 kDa)中,20℃孵育24小时,形成粘蛋白层。SPR测量使用SPR Navi™200仪器在模拟泪液(STF;23.1mM KCl, 20.0mM NaHCO3, 1mM CaCl2·2H2O, 113.5mM NaCl;pH 7.4),流速50 μL/min,温度22℃。
研究二
Kari等人(2016)测量了人类天然补体成分C3b (180 kDa)与修饰脂质体的相互作用动力学。涂有羧甲基葡聚糖水凝胶(6 kDa)的金传感器载玻片用十二烷基脂质锚点功能化,然后将脂质体固定在表面(图1.B)。研究了带和不带聚乙二醇的低聚胍基脂衍生物(OGD)带正电荷的脂质体。MP-SPR测量采用SPR Navi™200-L仪器(每个流道分别在670 nm和785 nm波长处),温度为20℃,流速为100 μL/min。所研究的C3b浓度分别为0.00833、0.0833和0.833 μM。使用TraceDrawer™和LayerSolver™软件对数据进行分析。
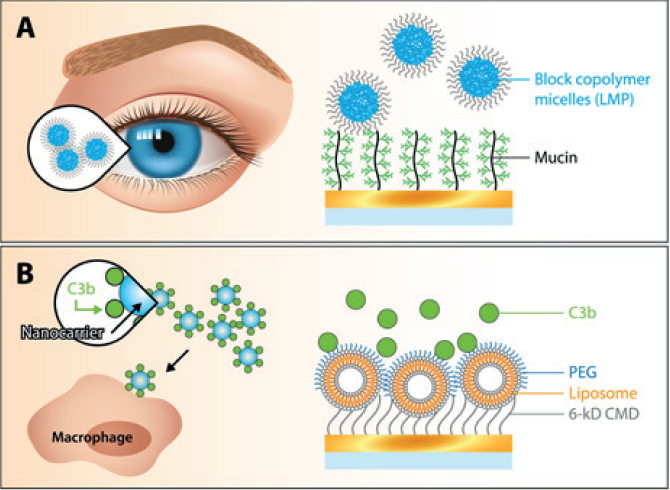
图1所示。(A)多参数表面等离子体共振(MP-SPR)测量纳米颗粒与表面固定化分子的结合:研究了嵌段共聚物胶束(LMP)与黏液表面的结合,用于黏液黏附眼部给药。(B)分子与表面附着纳米颗粒的结合:研究了调理剂C3b与改性脂质体基纳米颗粒的结合,以评估纳米载体的免疫反应。
结果和讨论
研究一
总的来说,主要目标是提高眼科药物的生物利用度。研究了黏附纳米载体以改善药物的眼部递送。随着纳米粒子PBA含量的增加,LMP胶束的黏附性增加,然而,表面出现饱和,因此额外的PBA并没有大大增加黏附性(图2)。结果表明,更高的PBA成分可能不会显著地对临床结果更有利。
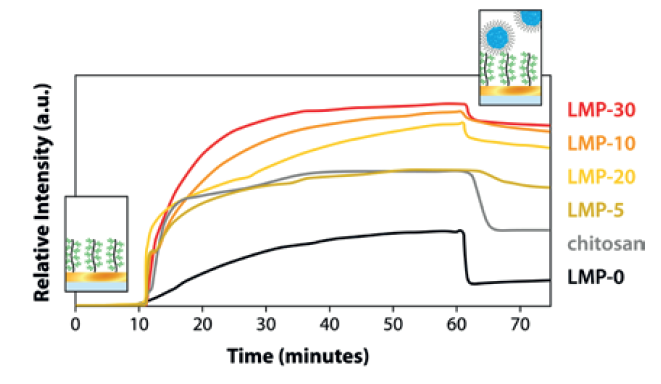
图2所示:测定了不同苯基硼酸(PBA)含量(LMP-0、-5、-10、-20和-30)的嵌段共聚物胶束与粘蛋白的结合。胶束的黏附力随PBA含量的增加而增加,并在LMP-10后达到平稳期。以壳聚糖与粘蛋白结合为阳性对照。在MP-SPR固定角度模式下进行测量。
研究二
研究了脂基纳米载体的免疫反应。与有PEG的脂质体表面相比,无PEG的OGD表面上C3b结合的MP-SPR响应明显更大(图3)。无PEG的OGD脂质体上C3b的表面质量密度(Γ)为~410 ~ 680 ng/cm2,聚乙二醇化脂质体上C3b的表面质量密度为Γ ~120 ~ 200 ng/cm2。C3b对OGD脂质体的亲和力KD = 3.8 × 10−8 M,对OGD + PEG脂质体的亲和力KD = 7.2 × 10−8 M明显较弱。由此可见,不含PEG的OGD脂质体诱导的活化相关反应较大。这可能导致补体系统(免疫系统的一部分)的表面诱导激活。
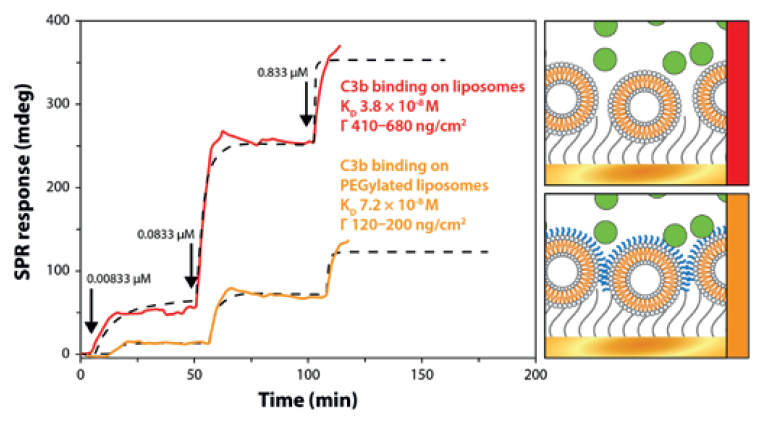
图3。C3b与低聚胍脂修饰(OGD)脂质体的结合。不含PEG的脂质体的结合明显更强。测量在MP-SPR的角扫描模式下进行。
除了相互作用外,还使用LayerSolver™软件测定脂质层厚度和折射率。OGD脂质体层厚40.4±9.3 nm,聚乙二醇化OGD脂质体层厚44.4±4.2 nm(图4)。
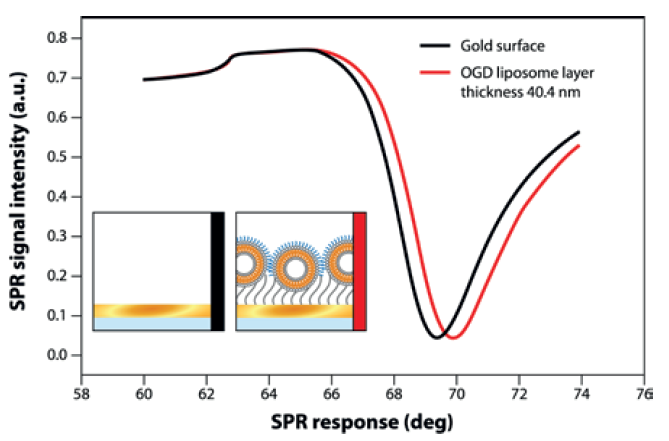
图4。测定脂质体沉积前后的全SPR曲线。使用LayerSolver™计算脂质体层的厚度(d)和折射率(n)。
结论
MP-SPR Navi™是纳米载体开发的优秀工具。它可以实时测量纳米粒子的相互作用,无需标记。MP-SPR还可以计算层厚度和折射率,这可以用来确保颗粒在表面的构象。MP-SPR方法基本上适用于测量任何材料,因此可以研究金属、聚合物和脂质纳米颗粒。使用纳米颗粒的检测可以被安排在传感器表面(图1B),或者它们可以自由地漂浮在修改后的传感器表面上方的缓冲流中(图1A),从而为检测开发提供了几种选择。
