- 概述
- 理由
- 解答问题
- 应用指南
- 发表文章
细胞外囊泡(EVs)作为潜在的治疗方法、药物输送系统和疾病(如癌症)的非侵入性诊断被广泛研究。探讨多参数表面等离子体共振(MP-SPR)仪器在卵巢癌早期检测中的应用:将肿瘤ev (SKOV-3)负载到表面固定化的LXY30肽上,基于MP-SPR测量,确定了相互作用的亲和常数、动力学常数、束缚质量和层厚。LXY30肽对表达α3β1整合素的ev具有高亲和力,为其诊断应用提供了可能。
简介
细胞外囊泡(EVs)是由人体细胞释放到体液中的纳米级膜囊泡。众所周知,它们在向周围细胞传递信号和促进细胞间甚至与远处细胞的通信方面发挥着重要作用。ev反映了亲本细胞的组成和状态,因此可以潜在地用作多种疾病(如癌症)的标志物。ev的膜特征可以通过整合素(跨膜糖蛋白)来表示,它影响细胞粘附、炎症、血栓形成和转移。特异性整合素在某些肿瘤细胞中过度表达,产生特征组合,因此是癌症诊断(检测)和治疗应用(即阻断整合素以减少转移)的有趣靶点。卵巢肿瘤细胞及其分泌的细胞外囊泡表达α3β1整合素。这种特殊的整合素可以被一种环状非肽LXY30靶向,LXY30已被开发用于检测ev。
通常,电动汽车的特点是各种技术需要标签和使用端点分析方法,而这些方法不能提供实时信息。然而,引入标签可能会改变颗粒的生化结构,从而影响结果。MP-SPR是一种实时、无标签、灵敏度极高的方法,可测量动态流动条件下的物理化学现象。因此,它可以被认为是表征细胞外囊泡相互作用的一种极好的方法。
经过验证的表面等离子体共振(SPR)检测方法广泛应用于不同的生物传感器研究,如评估分子相互作用的亲和力和动力学以及生物分子浓度的测定。多参数表面等离子体共振(MP-SPR)是研究多种靶标的良好平台。MP-SPR独特的光学配置使分析从小分子和抗体到纳米颗粒,甚至整个活细胞。特殊光学与强大的流体设置相结合,使MP-SPR不仅可以评估纯化样品,还可以评估粗样品,如牛奶,海水,血浆,血清和唾液。这些特点与生物传感器的发展密切相关,可用于生命科学领域的研究。
特别的是,MP-SPR不仅提供了相互作用的亲和力和动力学,还提供了同一实验中有关层性质和吸附质量的信息。由于测量是在一个非常宽的角度范围(40-78度)和在一个以上波长的光,厚度和折射率沉积层可以评估。
材料和方法
在MP-SPR实验之前,BioNavis标准金传感器载玻片被非原位涂覆一层自组装的生物素化烷烃硫醇(11-巯基-1-十一醇,MuOH)单层(SAM)。进入仪器后,在运行缓冲液TRIS-EDTA (25 mM TRIS, 1mM EDTA, pH 8.0)中设置基线信号,然后在两个通道中注射链霉亲和素。生物素化LXY30肽仅在一个通道中引入,留下第二个通道作为参考,不含肽。从最低浓度到最高浓度(3.4 × 109、5.7 × 109和1.7× 1010颗粒/ml)顺序注射,将卵巢癌细胞外囊泡SKOV-3加载到两个通道中。使用TraceDrawer™for MP-SPR Navi™和MP-SPR Navi™LayerSolver对数据进行分析。
结果和讨论
成功地从癌细胞培养上清中提取了细胞外囊泡,并对其进行了表征,以确认分离过程的成功。通过纳米颗粒跟踪分析(NTA),细胞外囊泡的浓度为1.70±0.11 × 1013个/ml,大小分布为177±87 nm。
通过MP-SPR确定表面结合肽(LXY30)与流动的细胞外囊泡(SKOV-3)的相互作用(图1)。使用TraceDrawer™软件的“两位点”结合模型分析相互作用,将其解释为两组肽分子与一个细胞外囊泡结合。本文对三种假设的电动汽车进行了评估,其中表面α3β1整合素的含量被评估为每颗粒总蛋白的1%,5%或10%。所有三个病例的亲和力表明SKOV-3颗粒与表面结合的LXY30配体的强结合(图2,表1)。在本研究中,仅测量了三种浓度的分析物,然而,通常建议测量五种或更多浓度来评估亲和力和动力学。
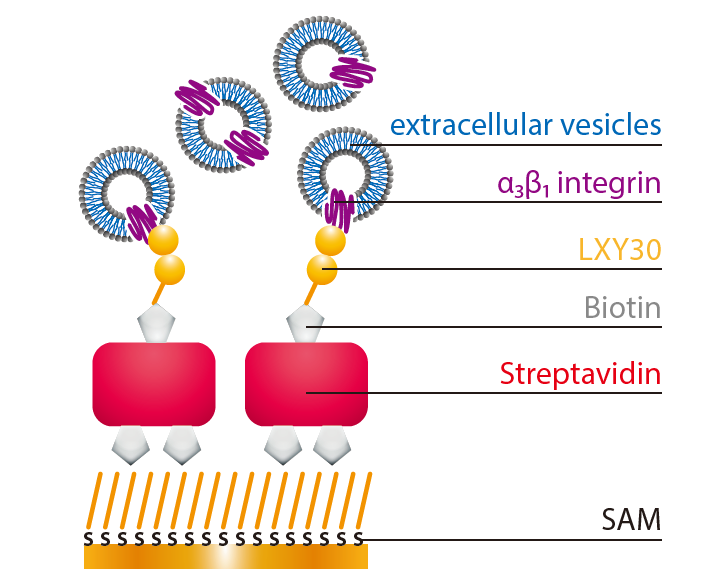
图1:细胞外囊泡与非肽的结合用于卵巢癌的早期检测。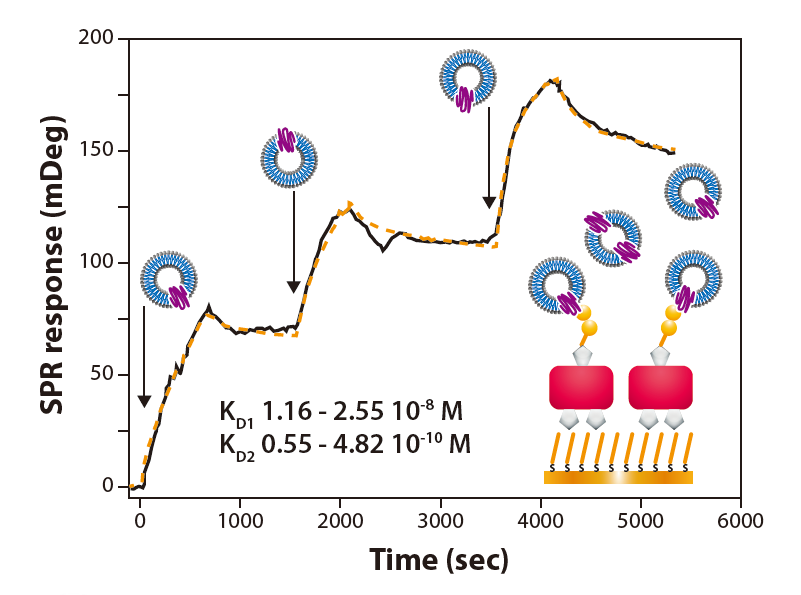
图2:使用TraceDrawer™对MP-SPR Navi™测定肽-细胞外囊泡相互作用的亲和力和动力学常数。黑色实线表示测量数据,橙色虚线表示连续注射α3β1整合素覆盖率分别为A) 1%, B) 5%和C) 10%的三种不同种群的电动汽车的传感图拟合。
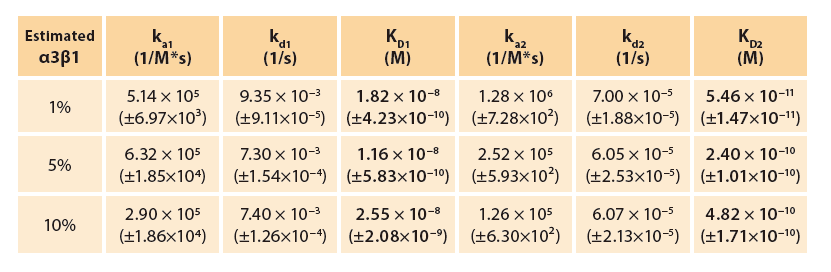
表1:SKOV-3颗粒与LXY30肽结合的亲和力和动力学常数。
通过在LayerSolver™软件中拟合完整的SPR曲线来评估吸附EV层的厚度和折射率(RI)(图3)。分析基于670和758 nm激光源提供的MP-SPR的多波长测量。表面结合的电动汽车的表面质量密度估计为90 ng/cm2。EV层的折射率为1.341,略高于PBS等缓冲水溶液的折射率。基于MP-SPR计算的外泌体层厚度仅为34 nm,而基于NTA的平均粒径为177±87 nm。这可能是因为MP-SPR提供了测量区域的平均厚度,而电动汽车在传感器上的分布不均匀。较低的厚度值很可能是由于结合在表面的外泌体之间的空隙造成的。此外,由于结合引起的ev形状变形可能解释了观测到的较低的厚度值。
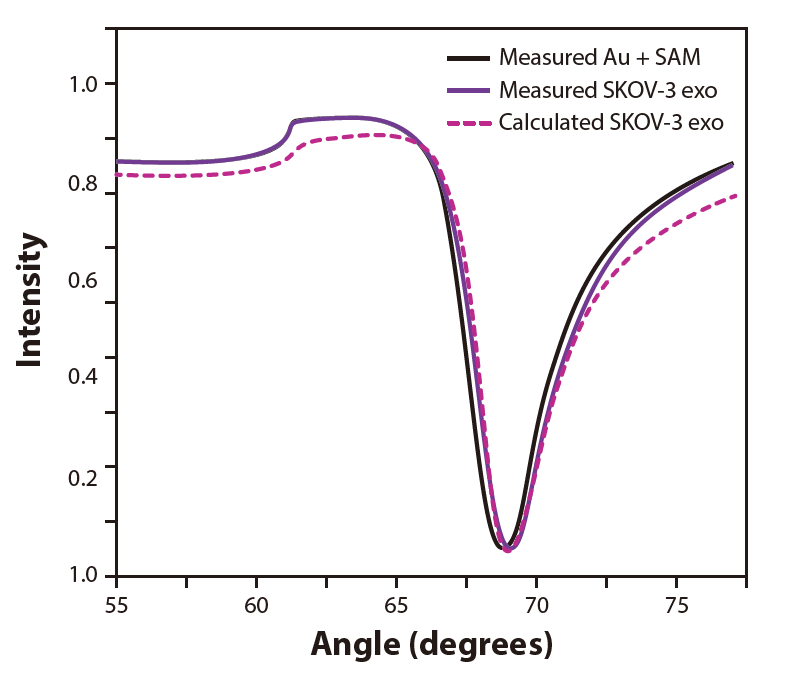
图3:利用LayerSolver软件分析SKOV-3细胞外囊泡吸附前后的全MP-SPR曲线,求解颗粒层厚度和折射率。进行了多波长分析,但为了表达清晰,这里只给出了670 nm的测量曲线。
结论
MP-SPR已被证明是表征细胞外囊泡相互作用的良好平台,如本例所示。单个MP-SPR测量提供了几个数值,如亲和和动力学常数、厚度、折射率和吸附质量,而实验是在无标记的方式下进行的。这里提出的方法不仅限于细胞外囊泡,而且适用于其他类型的纳米颗粒,包括聚合物和金属纳米颗粒。使用各种样品、表面和基质的可能性使MP-SPR成为生物传感器开发和生命科学研究的杰出平台。
